KAN YAPIMI (HEMATOPOEZ)
Olgun kan hücreleri göreceli olarak kısa yaşam döngüsüne sahip olduğundan hücre topluluğunun yerini sürekli olarak kan yapıcı, Hematopoetik (Gr. haima, kan, poiesis, bir yapım) organlarda üretilen kök hücre soyunun alması gerekmektedir. Embriyogenezin en erken evrelerinde, kan hücreleri Vilelius kesesi (yolk sae) mezoderminden gelişmektedir. Belirli bir zaman sonra, karaciğer ve dalak geçici hematopoetik dokular olarak görev yapar, fakat ilk ayın bitiminden sonra klavikula kemikleşmeye ve içinde kemik iliğini meydana getirmeye başlar. İskeletin geri kalanının doğum sonrası kemikleşmesi hızlandıkça, kemik iliği giderek artan ölçüde önemli bir hematopoetik doku haline gelir.Doğumdan sonra ve çocukluk çağına kadar, eritrositler, granüler lükositler, monositler ve trombositler kemik iliğine yerleşmiş olan kök hücrelerden oluşurlar. Bu hücrelerin oluşması ve olgunlaşması, sırasıyla, eritropoez, (Gr. erythros, kırmızı + poiesis), granülopoez, monositopoez ve megakaryositopoez olarak adlandırılır. Kemik iliği ayrıca Ienfoid organlara göç eden hücreleri de üretir. Olgunluğa erişmeden ve dolaşıma salınmadan önce, kan hücreleri özel farklılaşma ve olgunlaşma basamaklarından geçer. Bu olaylar sürekli olduğundan, çeşitli basamaklar arasında kalan, tipik özellikleri bulunan hücrelerle kan veya kemik iliği yaymalarında sıklıkla karşılaşılır.
KÖK HÜCRELER, BÜYÜME ETKENLERİ VE FARKLILAŞMA
Kök hücrelerin kendini yenileme özellikleri vardır ve bu hücreler çok yöne değişebilen pluripotent hücrelerdir. Bunların yavru hücrelerinin bazıları özel, geri dönüşümsüz olarak farklılaşan hücre tiplerini oluşturur ve diğer yavru hücreler kök hücre olarak kalır. Sabit bir sayıda (pluripotent) kök hücre bir havuzda korunur ve farklılaşma için toplanan hücrelerin yerini ise havuzda yavru hücreler alır. Hematopoetik kök hücreler, özel hücre yüzey antijenlerini işaretlemek için floresan etiketli antikorlar ile ve bir floresanla uyarılmış, hücre ayırıcı alet ile ayrılır. İn vivo teknikler; normal verici farelerin kemik iliğini, hematopoetik hücreleri ortadan kaldırılmış olan, öldürücü düzeyde radyasyon uygulanan farelere enjekte etme şeklindedir. Bu hayvanlarda, nakledilen kemik iliği hücreleri, dalakta hematopoetik hücre kolonileri oluşturur. İn vitro teknikler; kemik iliği stromasından köken alan bir hücre tabakası ile yapılan bir yarılattı doku kültürü medyumunun kullanımı şeklindedir. Bu aracı hematopoez için uygun mikro çevre koşullarını oluşturur. Bir dizi kapsamlı deneyden elde edilen veriler, bu uygun mikroçevrese) koşullar altında, büyüme ekenleriyle uyarılmanın çeşitli kan hücresi tiplerinin gelişimini etkilediğini göstermektedir.
PLURİPOTENT HEMATOPOETİK KÖK HÜCRELER
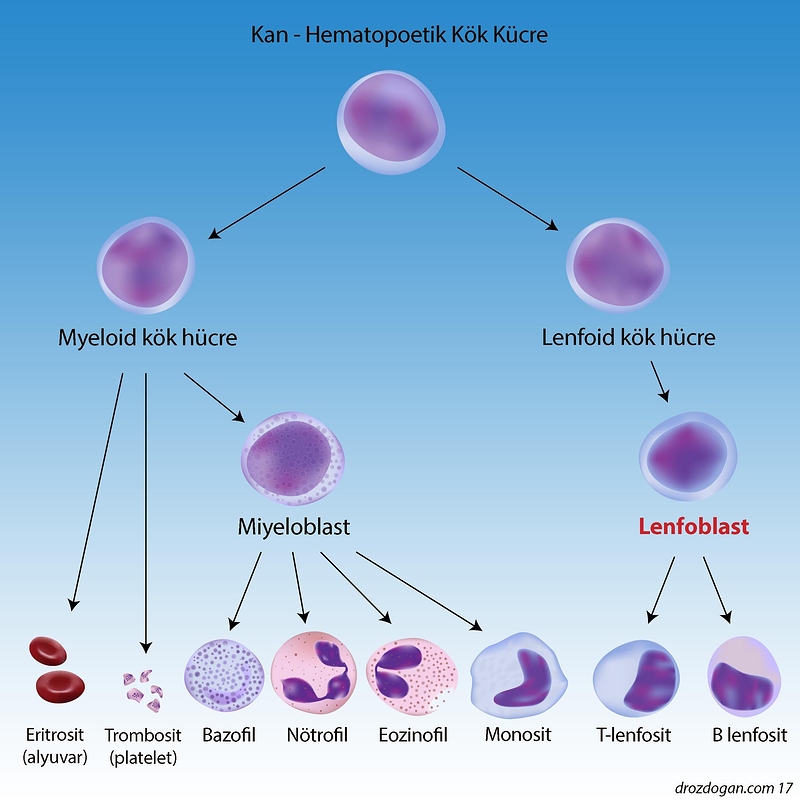
Bütün kan hücrelerinin kemik iliğinde tek bir hücre tipinden geliştiğine inanılmaktadır. Bu hücre tüm hücre tiplerini oluşturabildiğinden, pluripotent kök hücre olarak adlandırılır. Bu hücreler çoğalırlar ve lenfositler haline gelecek olan bir hücre dizisini ve kemik iliğinde gelişen miyeloîd hücreleri (granülositler, monositler, eritrositler ve megakaryositler) oluşturacak olan bir başka seriyi oluştururlar. Gelişimlerinin erken döneminde, Ienfoid hücreler kemik iliğinden, çoğaldıkları Limusa, lenf düğümlerine, dalağa ve diğer Ienfoid yapılara göç ederler.
Progenitor ve Prekürsör Hücreler
Çoğalma yetenekleri yüksek olan kök hücreler, bu yetenekleri kısıtlanmış yavru hücreleri oluştururlar. Bu unipotansiyel veya bipotansiyel progenitor hücreler, morfolojik özellikleri ilk defa dönüşecekleri olgun hücre tiplerini düşündürecek biçimde farklılık gösterdiği öncü, prekürsör hücreleri (blastlar) oluştururlar. Bunun tersi olarak, kök ve progenitor hücreler yapısal olarak ayırt edilemez ve lenfositleri andırırlar. Kök hücreler göreceli olarak küçük olan sayılarını sürdürecek kadar yeterli bir hızda bölünürler. Hücre bölünme hızı progenitor ve öncü hücrelerde artar ve çok sayıda farklılaşmış, erişkin hücreler üretilir (insan kemik iliğinde 3 X 109 eritrosit ve 0.85 X 1,09 granülosit/kg/gün). Progenitor hücreler bölünebilir ve hem progenitor hem de öncü hücreleri oluşturabilirken, öncü hücreler İse sadece erişkin kan hücrelerini oluşturur.
O halde kan yapımı ( hematopoez), farklılaşma ilerledikçe yetenekleri azalan kök hücrelerden oluşan hücrelerin eş zamanlı, sürekli çoğalması ve farklılaşmasının sonucudur. Bu olay çeşitli yeteneklere sahip kök hücrelerden köken alan hücre soylarının (koloni) ortaya çıktığı gerek in vivo, gerekse in vitro çalışmalarda gözlenebilir. Bir miyeloid kök hücreden köken alan soylar, hepsi aynı soydan olmak üzere; eritrositleri, granülositleri, monositleri ve megakaryositleri oluşturabilirler.Bu deneylerde, bazı türler sadece kırmızı kan hücrelerini (eritrositler) oluştururlar. Diğer soylar granülositleri ve monositleri oluşturur. Koloniler oluşturan hücreler koloni oluşturan hücreler (CFC) veya koloni oluşturan birimler (CFU) olarak adlandırılırlar. 13u çeşitli hücre soylarını isimlendirmede gelenek, her soyun ürettiği hücrenin baş harfini kullanmaktır. Buna göre; MCFC, bir monosit oluşturan koloniyi belirtir, ECFC eritrositleri oluşturur, MGCFC monositleri ve granülositleri oluşturur, vs. Kan yapımı uygun miniçevresel koşullara ve büyüme etkileyicilerinin varlığına bağımlıdır. Miniçevresel koşullar yeterli hücredışı matriks üreten, kanyapıcı oraganlartn stroma hücreleri ile donatılmıştır. Kan yapımına genel bir bakış, bu olay ilerledikçe, gerek farklılaşma yeteneğinin gerekse başlangıç hücrelerin kendini yenileme gücünün giderek azaldığını göstermektedir. Bunun tersi olarak, büyüme etmenlerine verilen mitotik yanıt giderek artarak, olayın ortasında en yükseğe erişir. Bu noktadan itibaren, mitotik yetenek düşer, yapısal özellikler ve işlevsel yeti gelişir ve olgun hücreler oluşturulur. Gerekli çevresel koşullar bir kez mevcut olduğu anda, kan hücrelerinin gelişimi hücre çoğalması ve farklılaşmasını etkileyen etmenlere bağımlı olur. Bu maddeler büyüme faktörleri, koloni stimüle edici faktörler (CSF), veya hematopoetinler (poetinler) olarak adlandırılır. Farkılılık gösteren kimyasal yapılara ve karmaşık, üst üste binen etkenliklere sahip olan büyüme faktörleri, başlıca olgunlaşmamış (çoğunlukla progenitor ve öncü) hücrelerin çoğalmasını uyararak (mitoza yönlendirme), erişkin hale gelen hücrelerin farklılaşmasını destekleyerek ve erişkin hücrelerin etkinliklerini artırarak işlev yapar. Az önce sözü edilen üç etkinlik aynı büyüme etmeninde var olabilir, ancak farklı büyüme etmenlerinde farklı yoğunluk seviyeleriyle de belirtilebilir. Çeşitli büyüme etmenlerine ait genlerin izolasyonu ve klonlanması hem yoğun büyüme faktörü üretimine hem de bunların in vivo ve in vitro etkilerinin çalışılmasına olanak tanır.

Klinik Bilgi
Büyüme etmenleri klinikte kemik iliği hücrelerinin içeriğini ve kan hücre sayımlarını artırmak için kullanılmaktadır. Büyüme etmenlerinin lökositlerin çoğalmasını artırmak için kullanılması klinik sağaltım açısından geniş yeni uygulamalara kapı açmaktadır. Büyüme faktörlerinin gizli iyileştirici kullanımları düşük kan sayımlarına neden olan hastalıklarda veya uyarılmış durumlarda (örn, kemoterapi, radyasyon) kan hücrelerinin sayısını artırmayı; hücre çoğalmasını artırarak ilik aktarımının (transplantlarının) etkinliğini artırmayı; kötü huylu kanserleri, enfeksiyöz ve immün yetmezlikli hastalıkları olan hastalarda konak savunmalarını artırmayı ve paraziter hastalıkların sağaltımını artırmayı kapsar. Hematopoetik hastalıklara genellikle, hematopoetik hücrelerin azalmış ya da aşırı üretimi ile sonuçlanan, bazı farklılaşmamış hücrelerin üretiminin baskılanması veya artırılması neden olur. Bununla birlikte; bazı hastalıklarda, birden fazla kök hücre tipinin çoğalmasının baskılanması ve artırılması, ardışık ya da eş zamanlı olarak meydana gelebilir. Bu tip durumlarda, bazı hücre tiplerinin sayılarında azalma (örn, kanyapıcı hücrelerin azalmış üretimi ile ayırt edilen bir hastalık olan aplastik anemi) ve aynı anda diğerlerinin sayılarında artış (örn, lökositlerin anormal protiferasyonu olan lösemi) söz konusudur. Öldürücü düzeyde radyasyon uygulanan farelere nakledilen normal kemik iliği ile yapılan başlangıçtaki deneyler, artık bazı kan yapıcı hücre büyümesi hastalıklarını iyileştirmek için sıkça kullanılan kemik iliği aktarılmasının (transplantasyonunun) temelini ortaya koymuştur.
KEMİK İLİĞİ
Normal şartlar altında, kemik iliği tarafından kan hücrelerinin üretimi, çok kısa bir sürede etkinliğini 7 katına çıkarmak suretiyle, vücudun gereksinimlerine göre ayarlanır. Kemik iliği uzun kemiklerin meduller kanallarında ve süngersi kemiklerin boşluklarında bulunur. Kaba incelemede, görünümlerine göre iki tip kemik iliği tanımlanmıştır; rengi kan ya da kan yapıcı hücrelerin varlığı ile oluşturulan kırmızı veya hematojenöz kemik iliği ve rengi çok sayıda yağ hücresinin varlığı ile oluşturulan sarı kemik iliği. Yeni doğanlarda, tüm kemik iliği kırmızıdır ve bu nedenle kan hücrelerinin üretimi açısından aktiftir. Çocuk büyüdükçe, kemik iliğinin çoğu giderek sarı tipe dönüşür. Ciddi kanama veya oksijensizlik (hipoksi) gibi belirli koşullar altında sarı kemik iliğinin yerini kırmızı kemik iliği alır.
Kırmızı Kemik İliği
Kırmızı kemik iliği bir stroma (Yunancadan, yatak anlamına gelir), kan yapıcı sütunlar hematopoetik kordonlar ve sinüzoidal kapillerlerden oluşmaktadır. Stroma 3 boyutlu bir retiküler hücre ağı ve kanyapıcı hücreleri ve makrolajları içeren ince bir retiküler lif ağıdır. Kemik iliğinin matriksi kollajen tip 1 ve III, fibronektin, laminin ve proteoglikanları içerir. Laminin, fibronektin ve bir başka hücre- bağlayıcı madde olan hemonektin, hücreleri matrikse bağlamak için hücre reseptörleri ile etkileşirler. Sinüzoicller bir endotelyal hücre tabakası tarafından oluşturulur. Dıştan kesintili bir retiküler hücre tabakası ve gevşek bir retiküler lif ağı sinüzoidal kapillerleri destekler. Olgun kan hücrelerinin ilikten salimini organizmanın ihtiyaçlarına yanıt olarak üretilen serbestleştirici etmenler taralından kontrol edilir. Komplemanın (immünolojik olarak aktif bir dizi kan proteini) C3 parçasını, hormonları (glukokortikoidler ve androjenler) ve bazı bakteriyel toksinleri kapsayan, serbestleştirici etkinliğe sahip çeşitli maddeler tanımlanmıştır. Kırmızı kemik iliğinin başlıca işlevleri, kan hücrelerinin üretimi, haşatlanmış kırmızı kan hücrelerinin yok edilmesi ve hemoglobinin yıkımından elde edilen demirin (makrofajlarda) depolanmasıdır.

DİĞER DOKULAR İÇİN BİR KÖK HÜCRE KAYNAĞI OLARAK KEMİK İLİĞİ
Klinik Bilgi
Önceki gözlemlerin tersine, kırmızı kemik iliği sadece kan hücreleri değil, çeşitli dokuları oluşturabilen kök hücrelerden de zengindir. Büyük farklılaşma yetenekleri ile, bu hücreler aynı kişinin iliğine ait kök hücrelerden üretilmelerinden dolayı vücut tarafından reddedilmeyen özelleşmiş hücreler meydana getirmeye olanak sağlar. Yöntem, kemik iliği kök hücrelerini toplamak, farklılaşmalarını transplantasyon amacıyla gereken hücre tipine yönlendirmek için onları uygun ortamda geliştirmek ve daha sonra doku kültüründen kaynaklanan hücreleri hastanın gereksinimi olan hücrelerin yerini atmaları için kullanmaktır. Bu durumda verici ve alıcı aynı kişidir ve histokompatibilite (doku uyumu) red olasılığını dışlayacak biçimde tamdır. Bu çalışmalar yeni başlamakta olmasına karşın, şimdiye kadarki sonuçlar umut vericidir.
ERİTROSİTLERİN OLGUNLAŞMASI
Erişkin bir hücre tüm özgül görevlerini yerine getirme yeteneğine sahip olduğu aşamada farklılaşmış olan hücredir. Olgunlaşmada temel olay hemoglobin sentezi ve çekirdeksiz, bikonkav, küçük gövdenin; eritrositin oluşumudur. Eritrositin olgunlaşması sırasında çeşitli önemli değişiklikler yer alır. Hücre hacmi azalır ve nükleolusların boyutları ışık mikroskobunda görünür duruma gelene kadar küçülür. Çekirdek çapı azalır ve kromatin, çekirdek yıkılmış bir görünüm sergileyene kadar giderek daha yoğun hale gelir ve sonunda hücreden çıkar. Sitoplazma içerisinde hemoglobin (asidofilik bir protein) miktarında eş zamanlı bir artış ile birlikte, poliribozomların sayısında kademeli bir azalma (bazofili azalır) söz konusudur. Mitokondri ve diğer organeller giderek kaybolur. Proeritroblast ile erişkin eritrosit arasında, araya giren 3-5 adet hücre bölünmesi vardır. Eritrositin, serinin ilk fark edilebilir hücresinden retikülositlerin kana salınımına kadarki gelişimi yaklaşık 7 gün sürer. Eritropoetin hormonu, demir, folik asit ve siyanokobalamin (vitamin B l2) eritrositlerin üretimi için gereklidir. Eritropoetin, böbreklerde üretilen, hemoglobin molekülünün protein komponenti olan globine ait mRNA’ nın üretimini uyaran bir glikoproteindir.
Farklılaşma
Eritrositlerin farklılaşması ve olgunlaşması, proeritrobkıstların, bazofilik eritroblastların, poiikromatofilik eritroblastların, ortokromatofilik eritroblastların (normoblastlar), retikülositlerin ve eritrositlerin oluşumunu içerir. Eritroid serideki ilk fark edilen hücre proeritroblasttır. Bu gevşek, danteliinsi kromatini ve net olarak görülebilen çekirdekleri ile büyük bir hücredir; sitoplazması bazofiliktir. Sonraki evre güçlü bir bazofilik sitoplazma ve görünen nükleolusu olmayan koyu bir çekirdek ile, bazofilik eritroblast (erythros + Gr. hlastos, germ) tarafından temsil edilir. Bu iki hücre tipinin bazofilisine, hemoglobin sentezinde rol alan çok sayıdaki poliribozom neden olur. Sonraki evre sırasında, poliribozomlar azalır ve sitoplazma alanları hemoglobin ile dolmaya başlar. Bu evrede boyama, hücrede çeşitli renklerin ortaya çıkmasına neden olur-polikromatofilik (Gr. polys, çok, + chrom a, renk, + pbilein, sevmek) eritroblast. Bir sonraki evrede çekirdek koyulaşmaya devam eder ve sitoplazmik bazofili belirgin değildir, ki bu da tek biçimli asidofilik bir sitoplazmaya neden olur ortokromatofilik (Gr. orthos, doğru, chrom a + pbilein) eritroblast. Bir an gelir, bu hücre bir dizi sitoplazmik çıkıntı verir ve ince bir sitoplazma tabakası ile kaplı olan çekirdeğini dışarı atar. Geride kalan hücrenin hala, brilliant cresyl blue boyası uygulandığında boyanmış bir ağ oluşturmak üzere birleşen az sayıda poliribozomu bulunur. Bu hücre, poliribozomlarını hemen kaybeden ve olgun bir eritrosit haline gelen retikülosittir.
GRANÜLOSİTLERİN OLGUNLAŞMASI
Granülositlerin olgunlaşma işlemi 2 organelde; azurofilik ve spesifik granüllerde toplanmış olan bir miktar proteinin sentezi ile ayırt edilen sitoplazmik değişiklikler ile meydana gelir. Bu proteinler art arda 2 evrede kaba endoplazmia retikulumu ve Golgi kompleksinde üretilir. İlk evre Wright veya Giemsa yöntemlerinde bazik boyalarla boyanan azurofilik grandilerin üretimine neden olur. İkinci evrede, spesifik granüllerde toplanmış olan çeşitli proteinlerin üretimi ile sentez etkinliğinde bir değişiklik meydana gelir. Bu granüller granülositlerin üç tipinin her birinde farklı proteinler içerir ve granülositin her tipinin çeşitli etkinliği için kullanılırlar. Bu olayda, gen ekspresyonunda belirgin biçimde bir kayma meydana gelerek nötrofillerin bakterileri ortadan kaldırmada özelleşmesine ve eozinofillerin ve bazofillerin yangısının ayarlanmasında rol oynamalarına olanak tanır.
GRANÜLOSİTLERİN OLGUNLAŞMASI
Miyeloblast miyeloid serilerdeki en olgunlaşmamış tanınabilir hücredir. İnce olarak dağılmış bir kromatini mevcuttur ve nükleoluslar görülebilir. Sonraki safhada, promiyelosit (L. pro, önce, + Gr. myelos, ilik, + kytos, hücre) bazofilik sitoplazması ve azurofilik granüllerle tanınır. Bu granüller lizozomal enzimler ve miyeloperoksidaz içerir. Promiyelosit, bilinen üç granülosit tipini meydana getirir. Farklılaşmanın ilk belirtisi, özel granüllerin miktar bakımından giderek arttığı ve sonunda sitoplazmanın çoğunu kapladığı miyelositlerde ortaya çıkar. Bu nötrofilik, bazofilik ve eozinofilik miyelositler nükleusun daha ileri koyulaşması ve özel granül içeriklerindeki kaydadeğer artış ile erişkin hale gelirler. Olgunlaşmayı tamamlanmadan önce, nötrofilik granülosit, nükleusunun eğri bir çubuk (band hücre) şeklinde olduğu bir anı safhadan geçer.
Klinik Bilgi
Çok sayıda olgunlaşmamış nötrofilin (band hücreler) kandaki görünümü sola kayma olarak adlandırılır ve klinik olarak belirgin olup, bakteriyel bulaşmayı gösterir.
NÖTROFİL ÜRETİMİNİN KİNETİĞİ
Bir miyeloblastın dolaşımda erişkin bir nötrofil olarak ortaya çıkması için geçen toplam süre 11 gün civarındadır. Normal şartlar altında, gelişimin miyeloblast, promiyelosit ve nötrofilik miyelosit safhalarında 5 mitotik bölünme meydana gelir. Nötrofiller çeşitli işlevsel ve anatomik kompartmanlardan geçer. Medüller oluşum kompartmanı bir mitotik kompartıman (~ 3 gün) ve bir olgunlaşma kompartmanı ( - 4 gün) olmak üzere alt bölümlere ayrılabilir. Medüller depo kompartmanı, gerektiğinde çok sayıda olgun nötrofil salıverme yeteneği olan bir tampon sistemi gibi etki eder. Nötrofiller yaklaşık 4 gün bu kompartımanda kalırlar. Dolaşım kompartmanı, plazmada asılı olan ve kan damarlarında dolaşan nötrofillerden meydana gelir. Marjinasyon kompartmanı, kanda mevcut olan fakat dolaşmayan nötrofillerden oluşur. Bu nötrofiller kapillerlerdedir ve vazokonstriksiyon ile geçici olarak dolaşımdan dışlanırlar, ya da özellikle akciğerlerde- endotelyuma yapışarak, ana kan akımında değil, damarların çevresinde olabilirler.
Marjinasyon ve dolaşım kompartımanları yaklaşık olarak eşit büyüklüktedir ve aralarında sabit bir hücre değişimi söz konusudur. Nötrofilin bu iki kompartımandaki yan-ömrü 6-7 saattir. Medüller oluşum ve depo kompartımanları birlikte dolaşım ve marjinasyon kompartmanlarının 10 katı civarındadır. Nötrofiller ve diğer granülositler kapillerlerin endotelyal hücreleri ile postkapiller venüller arasındaki intersellüler (hücreler arası) bağlantılardan geçerek (diapedez) bağ dokuya girerler. Bağ dokuları nötrofiller için beşinci bir kompartıman oluşturur, ancak bunun büyüklüğü bilinmemektedir. Nötrofiller burada 1-4 gün kalır ve daha sonra, majör fonksiyonları olan fagositozu yapmış olsalar da olmasalar da, apoptozis ile ölürler.
Klinik Bilgi
Kandaki nötrofillerin sayısındaki değişiklikler tüm bu kompartmanlar dikkate alınarak değerlendirilmelidir. Buna göre, dolaşımdaki nötrofillerin sayısında bir artış olan nötrofilinin, nötrofil üretimindeki bir artışı ifade etmesi gerekmez. Yoğun müsküler aktivite veya epinefrin uygulanması, marjinasyon kompartmanındaki nötrofillerin dolaşım kompartmanına hareket ederek, nötrofil üretimi artmamış olmasına rağmen belirgin bir nötrofiliye neden olmasına sebep olur. Ancak, glukokortikoidler (adrenal bez hormonları) ilikteki nötrofil prekürsörlerinin mitotik aktivitesini ve nötrofillerin kan sayımını artırırlar. Nötrofili ayrıca daha büyük sayıda nötrofilin medüller depo kompartmanından serbestleşmesi sonucu da meydana gelebilir. Bu nötrofili tipi geçicidir ve bunu nötrofillerin salınmadığı bir iyileşme dönemi takip eder. Bakteriyel enfeksiyonların seyri esnasında ortaya çıkan nötrofili nötrofillerin üretimindeki bir artışa ve bu hücrelerin medüller depo kompartmanında bulundukları sürenin daha kısa olmasına bağlıdır. Bu tip durumlarda, kan akımında band hücreler, nötrofilik metamiyelositler ve hatta miyelositler gibi olgunlaşmamış formlar meydana gelir. Bulaşma sırasında ortaya çıkan nötrofili, yoğun kas etkinliğinin bir sonucu olarak meydana gelenden daha uzun sürelidir.
LENFOSİTLERİN VE MONOSİTLERİN OLGUNLAŞMASI
Lenfositlerin ve monositlerin öncü hücrelerinin çalışılması, bu hücrelerin her ikisi de granülositlerin genç ve erişkin formları arasındaki ayrımı güçlendiren özel sitoplazmik granüller veya çekirdek boğumlanması içermediklerinden dolayı güçtür. Lenfositler ve monositler, başlıca yayma praparatlarda büyüklük, kromatin yapısı ve nükleolusların varlığı temel alınarak ayırt edilirler. Lenfosit hücreleri erişkin duruma geldikçe, kromatinleri sıkı, çekirdekleri görünür hale gelir, ve hücrelerin büyüklüğü azalır. Ek olarak, lenfositlerin alt gruplan farklılaşma sırasında, immünositokimyasal tekniklerle saptanabilen ayırt edici hücre yüzey reseptörleri kazanır.
Lenfositler
Dolaşımdaki lenfositler esas olarak timustan ve periferik lenfoid organlardan (örn, dalak, lenf nodları, tonsiller.) kaynaklanırlar. Bununla birlikte, tüm öncül lenfosit hücreleri kemik iliğinden kaynaklanır. Bu lenfositlerin bazıları T lenfositlerinin bütün niteliklerini kazandıkları timusa göç ederler. T lenfositleri periferik lenfoid organların özel bölgelerine yerleşirler. Diğer kemik iliği lenfositleri kemik iliğinde B lenfositlerine farklılaşırlar ve kendi özel bölmelerinde yerleştikleri ve çoğaldıkları periferik lenfoicl organlara göç ederler. Lenfoid hücrelerin ilk saptanabilen progenitörü, timidin ile birleşme ve prolenfositleri oluşturmak üzere 2 veya 3 kere bölünme yeteneğine sahip büyük bir hücre olan leııfoblasttır Prolenfositler daha küçüktür ve göreceli olarak daha sıkı kromatine sahiptir, fakat prolenfositleri T veya B lenfositleri olarak işaretleyen hücre yüzey antijenlerinin hiçbiri yoktur. Kemik iliğinde ve limusta, bu hücreler kökenlerinin özelliğini oluşturan hücre yüzey reseptörlerini sentezlerler, fakat rutin histolojik işlemlerde ayrı B veya T lenfositleri olarak tanınamazlar.
Monositler
Monoblast morfolojik özellikleri bakımından neredeyse miyeloblastın eşi olan bir öncü progenitor hücredir. Daha ileri farklılaşma, bazofilik bir sitoplazması ve büyük, hafifçe girintili bir nüklusu olan büyük bir hücre (8 nm çapına kadar) olan promonosite neden olur. Kromatin dantelimsi, nükleoluslar belirgindir. Promonositler monositlere gelişimlerinin seyri esnasında iki kere bölünürler. Büyük miktarda kaba endoplazma retikulumu, aynı zamanda granül yoğunlaşmasının meydana geldiğinin görüldüğü geniş bir golgi kompleksi mevcuttur. Bu granüller kan monositlerinde ince azurofîlik granüller olarak gözlenen primer lizozomlardır. Erişkin monositler kan dolaşımına girer, yaklaşık 8 saat dolaşır ve daha sonra makrofajlara olgunlaşırlar ve birkaç ay görev yaptıkları bağ dokularına girerler.
Klinik Bilgi
Hasta genellikte kansız ve bulaşmalara yatkındır. Lösemilerin ve diğer kemik iliği bozukluklarının çalışılmasında yardımcı olan bir klinik teknik kemik iliği aspirasyonudur. Kompak kemikten (genellikle sternumdan) bir iğne geçirilir ve ilik örneği çekilir. Örnek bir mikroskop lamına yayılır ve boyanır. Öncü kan hücrelerinin zarlarındaki proteinlere özel etiketli monoklonal antikorların kullanımı, bu kök hücrelerden köken alan hücre tiplerini saptamada yardımcı olur ve çeşitli lösemi tiplerinin daha kesin tanısına katkıda bulunur.
TROMBOSİTLERİN KAYNAĞI
Erişkinlerde, trombositler, sırayla megakaryoblastların değşmesi ile meydana gelen erişkin megakaryositlerin (Gr. nıegas, büyük + katyon, nükleus + kytos) sitoplazmasının parçalanması ile kırmızı kemik iliğinden kaynaklanırlar.
Megakaryoblastlar
Megakaıyoblast 15-50 //m çapındadır ve sayısız çekirdekçiği olan ovoid veya böbrek şeklinde bir çekirdeği bulunur. Çekirdek, trombositler oluşmaya başlamadan önce büyük ölçüde poliploid hale gelir (yani, normal bir hücrenin 30 katı kadar fazla DNA içerir). Bu hücrenin sitoplazması düzenli ve yoğun olarak bazofiliktir.
Megakaryositler
Megakaryosit düzensiz boğumlu bir çekirdek, kaba kromatin ve görünür çekirdekçikleri bulunmayan dev bir hücredir (35-150 //m çapında). Sitoplazma sayısız mitokondri, iyi gelişmiş bir kaba endoplazma retikulumıı ve geniş bir Golgi kompleksi içerir. Trombositlerin, Golgi kompleksinden köken alan, trombosit kaynaklı büyüme faktörü, fibroblast büyüme faktörü, von Villebrand faktörü (trombositlerin endotelyal hücrelere adezyonunu artırır) ve trombosit faktör IV (kan pıhtılaşmasını uyarır) gibi biyolojik olarak aktif maddeler içeren dikkat çekici grandileri bulunmaktadır. Megakaryosİtin olgunlaşması ile plazma zarının çok sayıda içe kıvrımları sitoplazmanın her tarafına dallanarak demarkasyon membranlarım oluşturur. Bu sistem trombositleri, dolaşıma atarak döken megakaryosit sitoplazması alanlarını tanımlar.
Klinik Bilgi
Kan trombositlerinin sayısının azaldığı bir hastalık olan trombositopenik purpuranın belirli formlarında trombositler megakaryositlerin sitoplazmasına bağlı görünür, ki bu da bu cisimciklerin serbestleşme mekanizmasındaki bir bozukluğu gösterir. Trombositlerin yaşam döngüsü yaklaşık olarak 10 gündür.